Коррозия меди и медных сплавов
Содержание:
- Химические свойства цинка
- Симптомы и признаки отравления
- Использование аммиака
- Основные инструменты
- Коррозийные свойства меди
- Влияние примесей на порчу металлов
- Коррозия в почве и влажном воздухе
- Способы окисления меди
- Как найти медь в Майнкрафт 1.17
- Что такое коррозия металлов и сплавов
- Коррозия меди в кислых средах
- Почему металл корродирует?
- Полезные советы и рекомендации по уходу за медными предметами
- Окисление меди в домашних условиях
- Состаривание с серым оттенком при помощи серной печени
- Применение меди
- Коррозийные свойства меди
- Химик.ПРО – решение задач по химии бесплатно
- В каких средах можно и нельзя использовать медь
- Свойства меди
- Что такое коррозия
- Классификация коррозионных процессов по условиям протекания коррозии.
Химические свойства цинка
Цинк Zn находится в IIБ группе IV-го периода. Электронная конфигурация валентных орбиталей атомов химического элемента в основном состоянии 3d104s2. Для цинка возможна только одна единственная степень окисления, равная +2. Оксид цинка ZnO и гидроксид цинка Zn(ОН)2 обладают ярко выраженными амфотерными свойствами.
Цинк при хранении на воздухе тускнеет, покрываясь тонким слоем оксида ZnO. Особенно легко окисление протекает при высокой влажности и в присутствии углекислого газа вследствие протекания реакции:
2Zn + H2O + O2 + CO2 → Zn2(OH)2CO3
Пар цинка горит на воздухе, а тонкая полоска цинка после накаливания в пламени горелки сгорает в нем зеленоватым пламенем:
При нагревании металлический цинк также взаимодействует с галогенами, серой, фосфором:
С водородом, азотом, углеродом, кремнием и бором цинк непосредственно не реагирует.
Цинк реагирует с кислотами-неокислителями с выделением водорода:
Особенно легко растворяется в кислотах технический цинк, поскольку содержит в себе примеси других менее активных металлов, в частности, кадмия и меди. Высокочистый цинк по определенным причинам устойчив к воздействию кислот. Для того чтобы ускорить реакцию, образец цинка высокой степени чистоты приводят в соприкосновение с медью или добавляют в раствор кислоты немного соли меди.
При температуре 800-900oC (красное каление) металлический цинк, находясь в расплавленном состоянии, взаимодействует с перегретым водяным паром, выделяя из него водород:
Цинк реагирует также и с кислотами-окислителями: серной концентрированной и азотной.
Цинк как активный металл может образовывать с концентрированной серной кислотой сернистый газ, элементарную серу и даже сероводород.
Состав продуктов восстановления азотной кислоты определяется концентрацией раствора:
4Zn + 10HNO3(0,5%) = 4Zn(NO3)2 + NH4NO3 + 3H2O
На направление протекания процесса влияют также температура, количество кислоты, чистота металла, время проведения реакции.
Цинк реагирует с растворами щелочей, при этом образуются тетрагидроксоцинкаты и водород:
С безводными щелочами цинк при сплавлении образует цинкаты и водород:
В сильнощелочной среде цинк является крайне сильным восстановителем, способным восстанавливать азот в нитратах и нитритах до аммиака:
Благодаря комплексообразованию цинк медленно растворяется в растворе аммиака, восстанавливая водород:
Также цинк восстанавливает менее активные металлы (правее него в ряду активности) из водных растворов их солей:
Zn + CuCl2 = Cu + ZnCl2
Zn + FeSO4 = Fe + ZnSO4
Симптомы и признаки отравления
Вначале рассмотрим острую интоксикацию солями меди. Типичная ситуация – это отказ от применения индивидуальных средств защиты при опрыскивании сельскохозяйственных культур раствором медного купороса, бордоской жидкостью или хлорокисью меди в дачных условиях.
Первым симптомом при проникновении соединений меди внутрь будут резкие боли в эпигастральной области, и даже симптомы желудочного кровотечения. Если произошло отравление медным купоросом, то рвотная масса может иметь голубоватый, или синеватый оттенок. Отравление солями меди в острой форме часто вызывает металлический вкус во рту, а также боли в грудной клетке.
Самый первый орган, который старается сдержать токсический удар меди и ее соединений – это печень. Острая интоксикация медным купоросом приводит к токсическому поражению печени, у пациентов развивается желтуха. Медь проявляет токсическое действие в отношении крови, поэтому желтуха возникает также вследствие гемолиза эритроцитов. Медь поражает ткань почек и легких.
При массивном поступлении соединений меди в кровь возникает острая почечная недостаточность, но вызванная не прямым токсическим действием меди на почки, а накоплением в крови гемоглобина, связанного с распадом эритроцитов. Он засоряет почечные канальцы и нарушает их структуру. В тяжелых случаях при острой интоксикации солями меди возникает выраженный сосудистый коллапс и развивается токсический шок.
Хроническое отравление медью может возникать и без всякой внешней интоксикации. Как это можно себе представить? Существует тяжелое врождённое заболевание, которое называется болезнью Вильсона-Коновалова, или гепатолентикулярной дегенерацией. В основе болезни лежит нарушение синтеза белка церулоплазмина. Как было сказано выше, церулоплазмин транспортирует медь в организме, и помогает ее утилизировать, разнося в необходимые органы и ткани.
Если возникает дефицит этого белка, то медь, поступающая в обычных концентрациях с пищей и водой, постепенно накапливается в организме, и приводит к очень тяжелым расстройствам. Возникают такие симптомы отравления медью у человека, как насильственные движения, тремор, повышенный мышечный тонус. Развиваются признаки паркинсонизма, психические нарушения. Это связано с длительным накоплением меди в так называемых базальных ганглиях, или центральных регуляторах координации непроизвольных движений и мышечного тонуса. Это заболевание встречается нечасто, один случай на 30000 человек. Характерным его признаком является обнаружение кольца из отложений металлической меди по периферии радужной оболочки глазного яблока (Кольцо Кайзер – Флейшера).
Отравление солями меди в хронической форме может произойти и у сельскохозяйственных рабочих. Примером может служить так называемая «болезнь опрыскивающих виноградники». При использовании бордоской жидкости для регулярного обработки сельскохозяйственных культур постепенно начинается изменение в легких в виде пневмосклероза. В основе этого патологического состояния лежит образование воспалительных гранулем, когда лейкоциты окружают попавшие в лёгкие частицы меди, а затем развивалась вторичная воспалительная реакция.
Также при хронической интоксикации длительное использование соединений меди приводит к возникновению цирроза печени, злокачественных новообразований в лёгких, а также злокачественных новообразований крови. Медь действует и местно. Аллергия на медь часто развивается даже у тех, кто носит медный браслет, но в производстве, когда контакт с металлической медью и ее соединениями может быть гораздо более выражен, симптомы аллергии на медь проявляются, прежде всего, раздражением глаз. Это коньюктивит, токсический кератит и другие симптомы.
В том случае, если интоксикация произошла парами меди при сварке цветных металлов, при длительной работе с медной пылью в цеху, то тогда возникает у пациента острая литейная лихорадка. Она была описана в соответствующих статьях, посвященных токсическим свойствам других металлов. Пациента беспокоит сухой кашель, головная боль. Появляется одышка, слабость, резко повышается температура до 40 градусов и выше. На коже возможно появление аллергической реакции в виде диффузной красной сыпи, которая сопровождается зудом.
Как помочь пациентам? Каково лечение отравления медью?
Использование аммиака
Из всех представленных средств аммиак является самым едким веществом, но он лучше всех может состарить медь и даёт патину коричнево-зелёного оттенка. Минусом применения этого средства является то, что этот газ испаряется, из-за чего обработку им нужно осуществлять чаще, чем другими веществами. Для использования этого способа понадобится: сам аммиак без примесей, герметичное пластиковое ведро, небольшие деревянные бруски.
https://youtube.com/watch?v=TRHd1wwZlbs
- на дно ведра положить бруски таким образом, чтобы получилась небольшая, но устойчивая платформа;
- налить в ведро аммиак, не доводя его уровень до верхней поверхности платформы;
- поставить на деревянную конструкцию медное изделие так, чтобы оно крепко держалось на платформе. Если же оно упадёт с неё, то его нужно просто достать, промыть водой и снова разместить на брусках;
- плотно закрыть ведро и проверять готовность каждый час. Обычно процедура занимает несколько часов. Во время проверки появления нужного оттенка нельзя вдыхать пары аммиака.
Покрывать лаком изделие не стоит, так как придётся периодически его снимать, потому что, как было сказано выше, обработка аммиаком осуществляется многократно в течение использования медной вещи.
Основные инструменты
Применение различных способов состаривания подразумевает использование некоторых инструментов или подручных средств. Но есть универсальные предметы, которые используются при любом методе:

Патинирование – это искусственное состаривание предметов интерьера из меди
- само изделие, тщательно обработанное;
- плотные резиновые перчатки;
- защитные очки для безопасности глаз;
- средство для состаривания (уксус, аммиак, приготовленные растворы, ацетон, нашатырный спирт);
- мыло или просто вода для очистки;
- магнит для проверки состава;
- горячая обработка (фен или любое другое нагревательное средство);
- кисть;
- специальная ёмкость (ведро, жестяные банки, пластиковые баночки);
- средства для полировки и шлифовки (губка, тряпочка).
Коррозийные свойства меди
Медь – металл с высокими пластическими свойствами, имеющий красно-золотистый цвет, а после удаления оксидной пленки – чуть розоватый. По электропроводности он уступает лишь серебру, также характеризуется высокой теплопроводностью. Благодаря низкому удельному сопротивлению медь применяется в электротехнике: идет на изготовление медных пластинок, проволоки, обмотки двигателей.
Из-за высоких антикоррозионных качеств металл включается в сплавы для улучшения их технических характеристик (бронза, латунь и другие). В гальванической среде медь становится катодом, вступает в электрохимические процессы и вызывает ускоренное ржавление прочих металлов.
Медь – неактивный химический элемент, поэтому практически не взаимодействует с воздухом, водой (пресной, морской). Если воздух сухой, на поверхности материала формируется оксидная пленка толщиной до 50 мн. Медное изделие темнеет, становится коричневым или зеленоватым, это называется патиной. В ряде случаев патина воспринимается как декоративное покрытие. Интенсивность коррозии низкая при контакте с разбавленной соляной кислотой, но при реакции с рядом иных кислот, с галогенами, «царской водкой» металл окисляется с образованием карбоната меди.
Влияние примесей на порчу металлов
Известно, что металлы в чистом виде практически не подвергаются коррозии. Но на практике все материалы содержат какое-то количество примесей. Как же влияют они на сохранность при эксплуатации изделий? Допустим, что имеется деталь, изготовленная из двух металлов. Рассмотрим, как происходит коррозия меди с алюминием. При нахождении на воздухе ее поверхность покрывается тончайшей пленкой из воды. Надо заметить, что вода разлагается на ионы водорода и гидроксид-ионы, а углекислый газ, растворенный в воде, образует угольную кислоту. Получается, что медь и алюминий, погруженные в раствор, создают гальванический элемент. Причем алюминий – анод, медь – катод (алюминий в ряду напряжений стоит левее меди).
Ионы алюминия попадают в раствор, а к меди переходят избыточные электроны, разряжая у ее поверхности ионы водорода. Ионы алюминия и гидроксид-тоны соединяются и откладываются на поверхности алюминия в виде белого вещества, вызывая коррозию.
Коррозия в почве и влажном воздухе
Разрушение меди в грунте происходит под влиянием кислот, содержащихся в почве, в отличие от воды насыщенные кислородом породы в меньшей степени окисляют металл. Наибольшую опасность для изделий из меди представляют живущие в почве микроорганизмы, точнее, продукты их жизнедеятельности.
Земля также как и вода подвергает медные трубы коррозии
Многие из них выделяют сероводород, который способен разрушить структуру металла. Изделие, которое находилось долгое время в земле, может полностью рассыпаться при изъятии.
Во влажном воздухе коррозия меди проявляется с течением длительного периода времени. Сухой климат вообще не влияет на разрушение металла. Влажный воздух насыщен углекислым газом, сульфидами, хлоридами – эти вещества вызывают коррозию металла, разрушая ее защитную пленку. При длительном пребывании изделия во влажном воздухе начинает образовываться слой патины – это оксид солей, он сначала имеет темно-коричневый цвет, затем приобретает зеленый оттенок. Патина не растворяется в воде и не подвержена влиянию влажности, а также нейтральна к меди, поэтому не только не разрушает ее, но и выполняет защитную функцию. На сегодняшний день существуют методы искусственного создания патины, их чаще всего используют художники и скульпторы, делая предметы, похожими на старинные вещи. Винтажный стиль в интерьере сейчас пользуется большой популярностью.
Способы окисления меди
Как ведет себя металл при контакте с воздухом
Окисление меди — естественный процесс. В периодической таблице Д. И. Менделеева медь расположена в группе «Металлы» под номером 29. Как и остальные металлы, она способна окисляться и образовывать устойчивые соединения в виде окисей и солей. Чтобы понять, что же такое окись меди, стоит приглядеться к старой бронзовой статуе. Со временем фигурка становится светло-зеленой из-за окисленной меди в составе бронзы. «Свежеизготовленная» бронзовая статуя окрашена в кирпичный цвет, но спустя время под действием влажного воздуха и углекислого газа протекает такая реакция:
Полученное сочетание соли и гидроксида меди — это малахит. Из него делают краски и всевозможные украшения.
Окислить медные изделия можно различными способами. В промышленности проводят анодное окисление с помощью электродов. Этот сложный и дорогостоящий процесс требует специального оборудования. В домашних условиях окислять медь гораздо проще.
Как найти медь в Майнкрафт 1.17
Чтобы получить медные слитки Minecraft, вам нужно найти медную руду. Этот ресурс появляется в форме медной жилы, что означает, что вы обычно найдете несколько блоков медной руды, сгруппированных вместе. Возьмите с собой каменную кирку или кирку более высокого качества, так как из медной руды, добытой с помощью деревянной кирки или другого предмета, ничего не выпадет.
Медная руда появляется с уровня y: 0 до y: 96, но с более высоким шансом появления вокруг средних слоев. Поэтому разумно начать поиск немного ниже уровня моря (y: 63). Если он появляется между слоями y: 0 и y: 16, медная руда примет форму глубинной сланцевой медной руды. Последняя имеет более высокий уровень твердости, чем обычная медная руда, и ее добыча занимает больше времени. Поскольку это также довольно редко, лучше всего выбрать обычную медную руду.
Что такое коррозия металлов и сплавов
Под коррозией понимают процесс разрушения металла под действием агрессивных факторов окружающей среды. В той или иной степени ржавеют все металлы, сплавы, в результате чего на них появляются ржавчина и участки нарушения целостности (дыры). Портиться со временем способны и неметаллы: примером можно назвать старение резины или пластика от взаимодействия с кислородом, при частых контактах с водой, перепадами температур.
Основной причиной коррозии считается термодинамическая неустойчивость металла к влиянию физических факторов или химических веществ, которые присутствуют в контактной среде. По сравнению с железом медь окисляется намного меньше, но при увеличении температуры этот процесс значительно ускоряется. При регулярном нахождении в среде с температурой выше +100 градусов любой металл ржавеет в несколько раз быстрее.
Коррозия меди в кислых средах
Медь проявляет хорошую устойчивость к коррозии в любых условиях, так как нечасто вытесняет водород, потому что она в электрохимическом ряду напряжений стоит около благородных металлов. Широкое использование меди в химической промышленности вызвано ее стойкостью ко многим агрессивным органическим средам:
- нитратам и сульфидам;
- фенольным смолам;
- уксусной, молочной, лимонной и щавелевой кислоте;
- гидроокиси калия и натрия;
- слабым растворам серной и соляной кислоты.
С другой стороны, отмечается сильное разрушение меди в:
- кислых растворах солей хрома;
- минеральных кислотах — хлорной и азотной, причем коррозия усиливается с увеличением концентрации.
- концентрированной серной кислоте, усиливаясь при повышении температуры;
- гидроокиси аммония;
- окисляющих солях.
Почему металл корродирует?
Жизнь современного человека нельзя представить без металлов. Они окружают нас везде — это и бытовая техника в наших домах, и транспортные средства, на которых мы добираемся до дома или работы, и смартфоны, без которых многие из нас не представляют жизнь. Почти всё, что нас окружает состоит из металлов, но, к сожалению, как и всё в этом мире, они не вечны и под действием внешней среды разрушаются — корродируют.
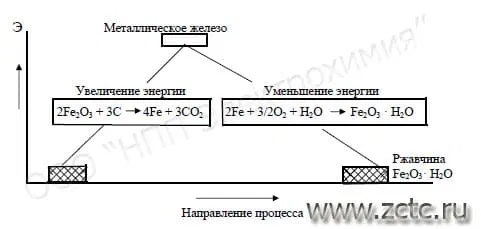
Почему коррозия «выгодна» для металлов? Дело в том, что большинство из них существуют в природе в химически связанном состоянии, например, в виде оксидов (корунд) или сульфидов (пирит). В чистом виде почти все металлы неустойчивы и чтобы выделить их из соединений приходится затрачивать немалую энергию. Обратный же процесс, когда металлы переходят в связанное состояние, всегда термодинамически более выгоден. Поэтому он происходит самопроизвольно, а металлы при любой возможности стремятся вступить в реакцию со своим окружением и перейти в более устойчивую форму. Иллюстрация этого представлена на рисунке 1.
Полезные советы и рекомендации по уходу за медными предметами
Стоит придерживаться следующих рекомендаций, чтобы сохранить блеск изделий из меди длительное время:
- Чтобы сохранить естественный медный блеск предметов продолжительное время, можно использовать защитное лаковое покрытие. Например, на дешевые медные украшения можно нанести прозрачный лак для ногтей. Такой способ позволяет изолировать изделие от контакта с воздушной атмосферой и кожей человека, что сохранит его блеск длительное время. Помимо лака для ногтей, также можно использовать пчелиный воск. Этот продукт можно встретить в соответствующих магазинах.
- Не используйте абразивные материалы и стальные предметы при очистке медного металла, поскольку они являются более твердыми, чем мягкая медь, и способны сильно поцарапать изделие.
- Тепло и влажность являются врагами медной посуды, поскольку значительно ускоряют ее разрушение и почернение. Чтобы избежать постоянного воздействия этих факторов, храните изделие в соответствующих условиях, например, в сухом проветриваемом шкафу.
- Не рекомендуется готовить пищу, содержащую много кислот, в медной посуде при высокой температуре. Содержащие кислоты продукты, например: уксус, фрукты, томаты и другие — наносят серьезный вред изделиям из меди.
- Большинство декоративных предметов покрыто защитным лаковым слоем. Такие предметы следует мыть только теплой водой с мылом и не использовать абразивные материалы, не полировать эти предметы, поскольку все это способно повредить защитное покрытие. Кроме того, изделия с защитным покрытием требуют специального ухода, поэтому рекомендуется следовать инструкциям производителя.
- Некоторая пищевая посуда из меди обладает защитным покрытием, которое необходимо снять перед использованием посуды по назначению. Снять покрытие можно двумя способами: поместить изделие в кипящую воду с небольшим количеством пищевой соды либо тщательно протереть изделие хлопчатобумажной тканью, смоченной в спирте или ацетоне, а после промыть под струей воды.
- Не стоит забывать вытирать медные изделия влажной чистой тряпкой, не позволяя пыли и грязи скапливаться на них.
Домашние методы очистки черноты на медных изделиях следует применять время от времени по мере необходимости, но нужно понимать, что с каждым разом предметы будут становиться тоньше.
Окисление меди в домашних условиях
Чтобы в полной мере понять, что такое окисление меди, проведем эксперимент. В домашних условиях получить окись меди несложно. Для этого понадобится:
- медная проволока;
- пассатижи;
- газовая или спиртовая горелка;
- раствор соляной кислоты;
- раствор этилового спирта;
- соль хлорида аммония;
- фаянсовая тарелка.
Итак, зажав медную проволоку пассатижами с одной стороны, вносим свободный конец проволоки в пламя горелки и прокаливаем на открытом огне. Благодаря высокой температуре горения, с течением времени медное изделие чернеет. В процессе химической реакции медь преобразуется в оксид:
Затем опускаем медную проволоку в раствор соляной кислоты. Сразу же видим, как бесцветный раствор становится бирюзовым. Такой цвет характерен для хлорида меди, который образуется в процессе реакции:
Медная проволока снова стала светло-кирпичной.
Также черная медная проволока восстанавливается с помощью этилового спирта. Для этого во флакон с этиловым спиртом опускаем медное изделие, и оно снова приобретет привычный золотистый цвет. Таким образом, в результате сложной химической реакции этиловый спирт окисляется до уксусного альдегида. Нажмите здесь, чтобы провести интересные опыты с медью.
Вернуть потемневшей медной проволоке первоначальный цвет можно также солью хлорида аммония.
При этом будет протекать химическое взаимодействие:
CuО + 2NH₄Cl = 2NH₃ + H₂О + CuCl₂
Для этого раскаленную проволоку опускаем на донышко фаянсовой тарелки с хлоридом аммония (NH₄Cl). В результате реакции будет выделяться газ аммиак, а потемневшее медное изделие снова приобретет рыжий оттенок.
Проводите химические эксперименты очень осторожно: аккуратно работайте с газовой или спиртовой горелкой, а также с соляной кислотой и другими агрессивными веществами. Источник
Источник
Состаривание с серым оттенком при помощи серной печени
Для начала вам нужно приготовить серную печень. Это можно сделать следующим образом:

Серная печень (полисульфид натрия)
- смешать порошок серы и поташ в составе 1:1 в жестяной банке, поставить смесь на огонь;
- после того как смесь начала плавиться и темнеть, начинается процесс спекания;
- через 15 минут жестяную банку нужно убрать с огня и дать смеси немного остыть.
Теперь можно приступать к подготовке раствора для того, чтобы начать патинирование и состарить медную вещь. Смешать 3 г соли и 3 г остывшей серной печени в 1 л воды. Тщательно перемешать раствор и опустить в него медное изделие. Когда медь приобрела необходимый серый оттенок, можно доставать изделие, затем промыть водой и высушить.
Применение меди
Благодаря ценным качествам медь и медные сплавы используются в электротехнической и электромашиностроительной отрасли, в радиоэлектронике и приборостроении. Существуют сплавы меди с такими металлами, как цинк, олово, алюминий, никель, титан, серебро, золото. Реже применяются сплавы с неметаллами: фосфором, серой, кислородом. Выделяют две группы медных сплавов: латуни (сплавы с цинком) и бронзы (сплавы с другими элементами).
Медь обладает высокой экологичностью, что допускает её использование в строительстве жилых домов. К примеру, медная кровля за счёт антикоррозионных свойств, может прослужить больше ста лет без специального ухода и покраски.
Медь в сплавах с золотом используется в ювелирном деле. Такой сплав увеличивает прочность изделия, повышает стойкость к деформированию и истиранию.
Для соединений меди характерна высокая биологическая активность. В растениях медь принимает участие в синтезе хлорофилла. Поэтому её можно увидеть в составе минеральных удобрений. Недостаток меди в организме человека может вызвать ухудшение состава крови. Она есть в составе многих продуктов питания. К примеру, этот металл содержится в молоке
Однако важно помнить, что избыток соединений меди может вызвать отравление. Именно поэтому нельзя готовить пищу в медной посуде
Во время кипячения в пищу может попасть большое количество меди. Если же посуда внутри покрыта слоем олова, то опасности отравления нет.
В медицине медь используют, как антисептическое и вяжущее средство. Она является компонентом глазных капель от конъюнктивита и растворов от ожогов.
Коррозийные свойства меди
Медь – металл с высокими пластическими свойствами, имеющий красно-золотистый цвет, а после удаления оксидной пленки – чуть розоватый. По электропроводности он уступает лишь серебру, также характеризуется высокой теплопроводностью. Благодаря низкому удельному сопротивлению медь применяется в электротехнике: идет на изготовление медных пластинок, проволоки, обмотки двигателей.
Медь – неактивный химический элемент, поэтому практически не взаимодействует с воздухом, водой (пресной, морской). Если воздух сухой, на поверхности материала формируется оксидная пленка толщиной до 50 мн. Медное изделие темнеет, становится коричневым или зеленоватым, это называется патиной. В ряде случаев патина воспринимается как декоративное покрытие. Интенсивность коррозии низкая при контакте с разбавленной соляной кислотой, но при реакции с рядом иных кислот, с галогенами, «царской водкой» металл окисляется с образованием карбоната меди.
Химик.ПРО – решение задач по химии бесплатно
Как протекает коррозия меди в атмосферных условиях? Чем вызвано образование зеленого налета на медных изделиях после длительного пребывания на воздухе? Чем можно объяснить преобразование зеленого в черный налет после нагревания меди?
Решение задачи
Рассмотрим, как протекает коррозия меди в атмосферных условиях.
В зависимости от состава среды и еще многих факторов на медной поверхности в атмосфере сначала образуется очень тонкая защитная пленка, состоящая с оксидов меди и ее чистой закиси. Время образования этой пленки может достигать нескольких лет. Поверхность немного темнеет, становится коричневатой. Иногда пленка может быть почти черного цвета (во многом зависит от состава коррозионной среды). После образования оксидного слоя на поверхности начинают скапливаться соли меди, имеющие зеленоватый оттенок. Коррозия меди
Образующийся оксид меди и соли называют еще патиной. Цвет патины колеблется от светло-коричневого, до черного и зеленого. Цвет патины зависит от качества обработки поверхности, состава самого металла и среды, времени контакта с коррозионной средой (от внутренних и внешних факторов). Коррозия меди. Закись меди – красно-коричневого цвета, окись – черного. Голубые, зеленые, синие и другие оттенки патины обуславливаются различными медными минералами (сульфаты, карбонаты, хлориды и др.). Патина по отношению к основному металлу нейтральна, т.е. не оказывает на медь вредного влияния (кроме хлористой меди). Соли и оксиды, формирующие патину, нерастворимы в воде и обладают естественными декоративными, защитными свойствами по отношению к поверхности меди. Коррозия меди
В атмосферных условиях, под действием кислорода медь окисляется, в результате чего образуется оксид меди (I) (закись меди):
Цвет этого соединения коричнево-красный.
При дальнейшей оксидации образуется чёрный оксид меди (II):
Коррозия меди. Электроны двигаются от меди к кислороду. Вывод: происходит окисление меди и на поверхности изделия образуется оксидная пленка.
Эти соединения защищают металл, но лишь в том случае, если оксидная плёнка не повреждена другими включениями. При этом оксид меди (II) является наиболее устойчивым.
Влажность и углекислый газ после длительного пребывания на воздухе вызывают образование зеленого налета на медных изделиях – карбаната меди и гидрооксида меди (смесь их называется малахитом):
После нагревания меди преобразование зеленого в черный налет обусловлено разложением малахита (зеленый) и получением оксида меди (II) (черный):
Источник
В каких средах можно и нельзя использовать медь
При правильной обработке, материал прослужит без коррозии более 100 лет
Но важно понимать, где медь будет устойчива к катализаторам коррозии, а где есть большой риск ее появления
Безопаснее всего применять материал на открытом воздухе и в пресной воде, вне зависимости от степени охлаждения или нагрева. В морской воде материал также долго остается неповрежденным и сохраняет свои эксплуатационные характеристики.
Опасность потенциально может появляться в том случае, если в почве, воде или воздухе есть много сероводорода, присутствует угольная кислота, соли тяжелых металлов, амины.
Когда вода сильно аэрирована, также возникает значительная опасность ударной коррозии и других видов постепенного разрушения.
Потому при покупке такого материала очень важно понимать, где вы будете использовать медное изделие, и какие внешние угрозы будут действовать на него в процессе эксплуатации
Свойства меди
Медь — это переходный элемент с ярко выраженными пластическими свойствами. Имеет золотистый цвет, а при отсутствии оксидной пленки — с добавлением розового. Это первый металл, который начал использовать человек. Латинское наименование элемента Cuprum (древн. Aes cuprium, Aes cyprium) произошло от названия острова Кипр, где в древности медь добывалась. Второе название — Aes, в переводе с латыни означает «руда» или «рудник».
Пластичный металл широко используется человеком.
- На воздухе металл покрывается оксидной пленкой, которая придает ему отличительный красно-желтый цвет. Медь вместе с золотом, осмием и цезием имеет преимущественно яркую окраску, что отличает их от других металлов, имеющих серебристый или серый цвет. Этот металл имеет высокую теплопроводность, а по электропроводности уступает только серебру.
- Медь характеризуется высокими коррозионными качествами и не реагирует с водой и разбавленной соляной кислотой. Окисляется «царской водкой», галогенами, кислородом. На воздухе с повышенным содержанием влаги металл окисляется и образует карбонат меди, который составляет верхний слой патины. Процесс образования защитной оксидной пленки на открытом воздухе длителен и может продолжаться несколько лет. В результате этого поверхность металла темнеет и приобретает коричневатый оттенок. После образования пленки на металле появляются соли меди, имеющие зеленоватую окраску. Оксид меди и соли называется патиной. Цвет ее изменяется от коричневатого до зеленого и черного и зависит от многих внешних факторов. Патина нейтральна к меди и наделена защитными и декоративными свойствами.
- Имея низкое удельное сопротивление, этот металл широко используется в электротехнике. Из него делают проволоку, идущую на изготовление обмоток электродвигателей. Листовой материал идет на изготовление различных элементов электрических аппаратов. Наличие в составе металла даже небольшого количества примесей значительно снижает его электропроводность.
- Медь используется для производства сплавов. На ее основе изготовляются латунь, бронза, дюралюминий и др. Благодаря высоким антикоррозионным характеристикам они широко используются для плакировки металлов с целью уменьшения коррозионного износа.
Что такое коррозия
Это разрушение металлов в результате воздействия на них окружающей среды. В странах с хорошо развитой промышленность ущерб от коррозии составляет 4–5% национального дохода. Портятся не только металлы, но и механизмы, и детали, изготовленные из них, что ведет к очень большим затратам. В результате ржавления трубопроводов зачастую происходит утечка вредных химических веществ, что приводит к загрязнению почвы, воды и воздуха. Все это пагубно сказывается на здоровье людей. Коррозия меди является спонтанным ее разрушением под влиянием отдельных элементов среды обитания человека. Причина порчи металла заключается в неустойчивости его к отдельным веществам, находящимся в воздухе. Скорость коррозии тем больше, чем выше температура.
Классификация коррозионных процессов по условиям протекания коррозии.
- Газовая коррозия протекает в газовой фазе с минимальным количеством влаги. Данная коррозия возникает при контакте металлов с агрессивными газами (галогены, кислород, оксид серы).
- Атмосферная коррозия протекает в атмосфере воздуха или другого влажного газа.
- Жидкостная коррозия – это коррозия, протекающая в различные рода жидкостях.
- Подземная коррозия – это коррозия металла, возникающая в следствии неоднородностей почвы, грунта.
- Коррозия в условиях криптоклимота происходит в условиях замкнутого пространства.
- Радиационная коррозия вызвана действием радиационного излучения.
- Морская коррозия возникает из-за депассивирующего свойства ионов хлора.
- Структурная коррозия связанна со структурной неоднородностью металлов.
- Коррозия, возникающая под действием блуждающих токов.